新规落地!国家药监局发布《牙膏备案资料管理规定》
时间线
- 2023.3.16
国家药监局公布了《牙膏监督管理办法》,宣布2023年12月1日起正式实施。
- 2023.9.25
国家药监局发布了《牙膏备案资料管理规定(征求意见稿)》;
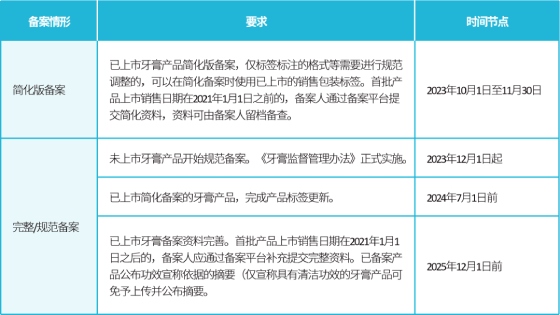
国家局发布2023年第124号公告,即 “关于贯彻落实牙膏监管法规和简化已上市牙膏备案资料要求等有关事宜的公告”, 明确了牙膏简化及完整/规范备案要求。
- 2023.11.22
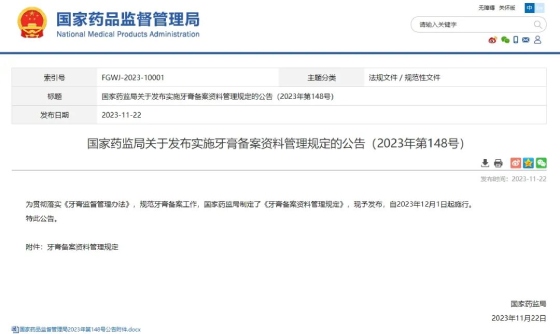
国家药监局发布关于发布实施牙膏备案资料管理规定的公告,《牙膏备案资料管理规定》(以下简称《规定》),自2023年12月1日起施行。
《规定》包含哪些内容


一、牙膏产品配方要求
- 配方填报总体要求
产品配方为生产投料配方,备案人按照国家药监局发布的牙膏相关技术规范标准和技术指导原则,或者参照化妆品相关技术规范标准和技术指导原则进行填报。

- 多配方填报要求
包含两个或者两个以上独立配方且包装容器不可拆分的牙膏,应当分别填写配方,按一个产品进行备案。
- 原料安全相关信息
主要包括原料质量规格、安全性风险物质控制、原料安全风险评估结论等与原料安全相关的信息。
- 牙膏新原料的使用
需填写使用新原料的注册证号或备案号,提交新原料注册人备案人允许使用新原料的授权文件。
二、产品执行的标准
总体要求, 产品执行的标准,应当符合国家有关法律法规、强制性国家标准和技术规范的要求(编制要求及示例可参考《规定》的附件1、2),其内容主要为:

三、标签要求
备案人应当提交产品标签样稿,上传产品销售包装及说明书。产品标签中标注的内容、标注方式和格式等应当符合《牙膏监督管理办法》《化妆品标签管理办法》等的要求。
四、牙膏检测报告
牙膏进行备案时,备案人应当提交产品检验报告,一般包括微生物与理化检验报告、毒理学试验报告、功效评价报告等。
(一)微生物与理化检验:
微生物与理化检验的受检样品应当为同一批号产品。
微生物和理化检验项目应当符合《检验项目要求》的要求,优先选择《化妆品安全技术规范》收录的检验方法。
除如微生物及重金属等常规项目参照《化妆品安全技术规范》外, 牙膏产品需根据具体产品进行PH值、对口腔硬组织的安全评价、过硬颗粒、总氟、可溶氟、游离氟、二甘醇和乙二醇、甲醇、二恶烷、游离甲醛等进行测试。
(二)毒理学试验:
部分牙膏的产品检验报告需包括口腔黏膜刺激试验项目,优先选择《化妆品安全技术规范》收录的试验方法,或者参考相关口腔医疗器械试验方法。
可免于提交该产品的口腔黏膜刺激试验报告情形:生产企业已取得所在国家(地区)政府主管部门出具的生产质量管理体系相关资质认证,且产品安全风险评估结果能够充分确认产品安全性的。
不豁免提交产品口腔黏膜刺激试验报告:

(三)功效评价:
宣称清洁以外其他功效的,需进行人体功效评价或者其他功效评价,备案人根据功效评价结果编制并公布功效宣称评价摘要;
宣称具有防龋、抑牙菌斑、抗牙本质敏感、减轻牙龈问题等功效,需进行人体功效评价;
通过添加氟化物达到防龋功效,且含氟量达到《检验项目要求》的,可免于功效评价防龋;
牙膏仅宣称清洁功效的,可免于功效评价。
(四)安全评估报告:
备案人应当参照《化妆品安全评估技术导则》的有关原则和要求,结合牙膏产品实际情况,科学合理开展产品安全评估,并提交产品安全评估报告。
如化妆品安全评估报告编制要求, 牙膏安全评估报告应包含:
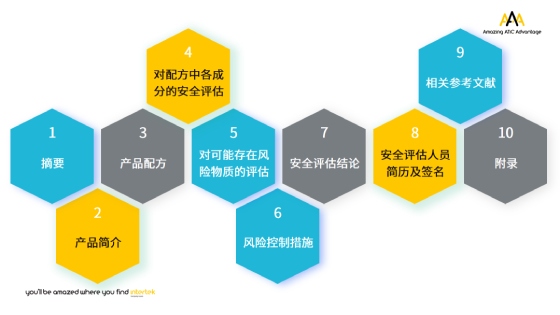
无法通过公开数据资料确认配方成分的安全性,还可通过以下其中一种方式完善产品安全评估资料,且该评估资料应当符合国家药监局发布的牙膏、化妆品相关技术规范标准和技术指导原则:

五、儿童牙膏
- 定义
儿童牙膏是指宣称适用于年龄在12岁以下(含12岁)儿童的牙膏;
- 功效宣称
儿童牙膏可以宣称的功效类别仅限于清洁、防龋;
- 配方设计原则 & 安全评估
儿童牙膏应当考虑儿童生理特点, 配方设计原则应当遵守安全优先、功效必须、配方极简原则, 安全评估过程需体现配方设计原则,且在危害识别、暴露量计算等方面,应当考虑儿童的生理特点。
温馨提示
《牙膏监督管理办法》实施在即。牙膏备案人应当根据《规定》要求, 尽快准备牙膏产品的备案资料,并根据本文中的时间节点要求, 完成对牙膏产品备案的要求。
关于Intertek天祥集团
Intertek是全球领先的全面质量保障服务机构,始终以专业、精准、快速、热情的全面质量保障服务,为客户制胜市场保驾护航。凭借在全球100多个国家的1,000多家实验室和分支机构,Intertek致力于以创新和定制的保障、测试、检验和认证解决方案,为客户的运营和供应链带来全方位的安心保障。
详情请登录:www.intertek.com.cn
